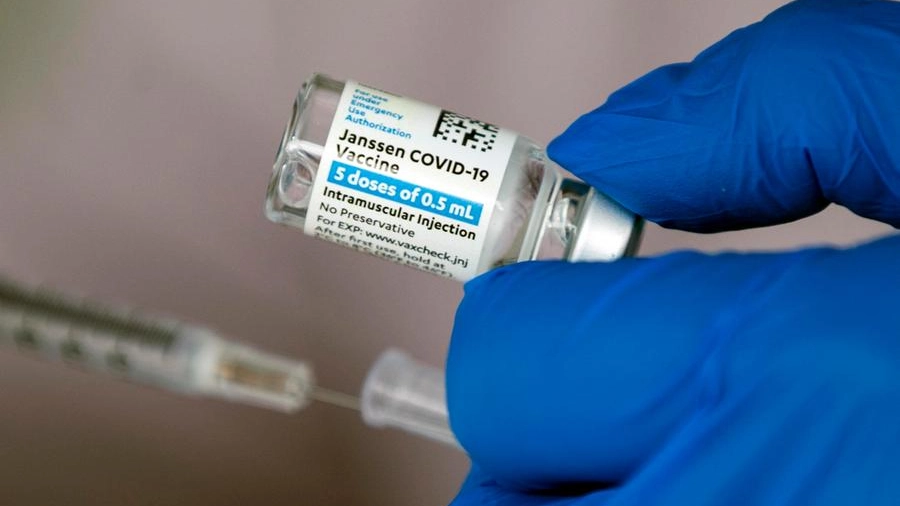
Vaccino Johnson & Johnson
Casi di trombosi dopo aver ricevuto dose di vaccino. Dopo il caso AstraZeneca era esploso, dagli Stati Uniti, quello di Johnson&Johnson, il vaccino monodose che avrebbe dovuto debuttare in questi giorni e su cui subito si sono addensate delle nubi. La palla era passata ad Ema che aveva annunciato le sue verifiche. Ora l'Agenzia europea del farmaco fa sapere che scioglierà le riserve martedì 20 aprile. In un briefing convocato dall'ente Ue, verranno rese note le conclusioni del comitato di farmacovigilanza Prac che sta esaminando gli eventi tromboembolici post iniezione scudo segnalati per questo vaccino anti Covd. In Europa il lancio del prodotto è stato messo in stand by dalla stessa zienda, proprio in attesa dell'esito delle valutazioni in corso.
Il 4 aprile le agenzie sanitarie federali americane hanno chiesto una pausa immediata nell'uso del vaccino di Johnson&Johonson dopo che sei persone avevano hanno sviluppato una rara forma di malattia da coaguli nel sangue "entro circa due settimane dalla vaccinazione". E' emerso che si trattava sempre di donne, di età compresa tra i 18 e i 48 anni. Una di loro è morta e una seconda donna in Nebraska è stata ricoverata in condizioni critiche. Sei casi su circa 7 milioni di dosi effettuate con il monodose, ma tanto è bastato a fermare la distribuzione del siero negli States e a valanga anche in Europa.
Nel caso di AstraZeneca, l'Ema ha sempre sottolineato che "i benefici sono superiori ai rischi". Ma via via la maggior parte dei Paesi europei ha preferito la strada della prudenza, limitando il siero agli over 60. C'è chi, come la Danimarca, ha deciso di farne definitivamente a meno. La Commissione europea presieduta da Ursula von der Leyen ha nel frattempo annunciato che dal 2022 abbandonerà i vaccini ad adenovirus vettore (come AstraZeneca e J&J) a vantaggio di quelli a mRna come Pfizer (con cui sta già negoziando un terzo contratto), Moderna e, quando sarà disponibile, CureVac.

